مقالة علمية لرئيس قسم الكيمياء الحياتيه بعنوان دور الطرد المركزي التحليلي في دراسة اضطرابات تجمع البروتينات كمؤشرات لأمراض التنكس العصبي
تُعد أمراض التنكس العصبي من أكثر الاضطرابات تعقيدًا من الناحية الجزيئية، إذ تتميز بحدوث خلل في طيّ البروتينات يؤدي إلى تكوّن تجمعات غير طبيعية داخل الخلايا العصبية أو في محيطها. وتكمن خطورة هذه التجمعات في كونها تبدأ غالبًا بتكوين وحدات أوليغوميرية صغيرة ذات سمّية عالية قبل تشكّل اللويحات الليفية الكبيرة.
من أبرز الأمراض المرتبطة باضطرابات تجمع البروتينات:
Alzheimer's disease
Parkinson's disease
حيث يرتبط الأول بتجمع بروتين الأميلويد بيتا وبروتين تاو، بينما يرتبط الثاني بتراكم بروتين ألفا-سينوكلين.
الآليات الجزيئية لتجمع البروتينات
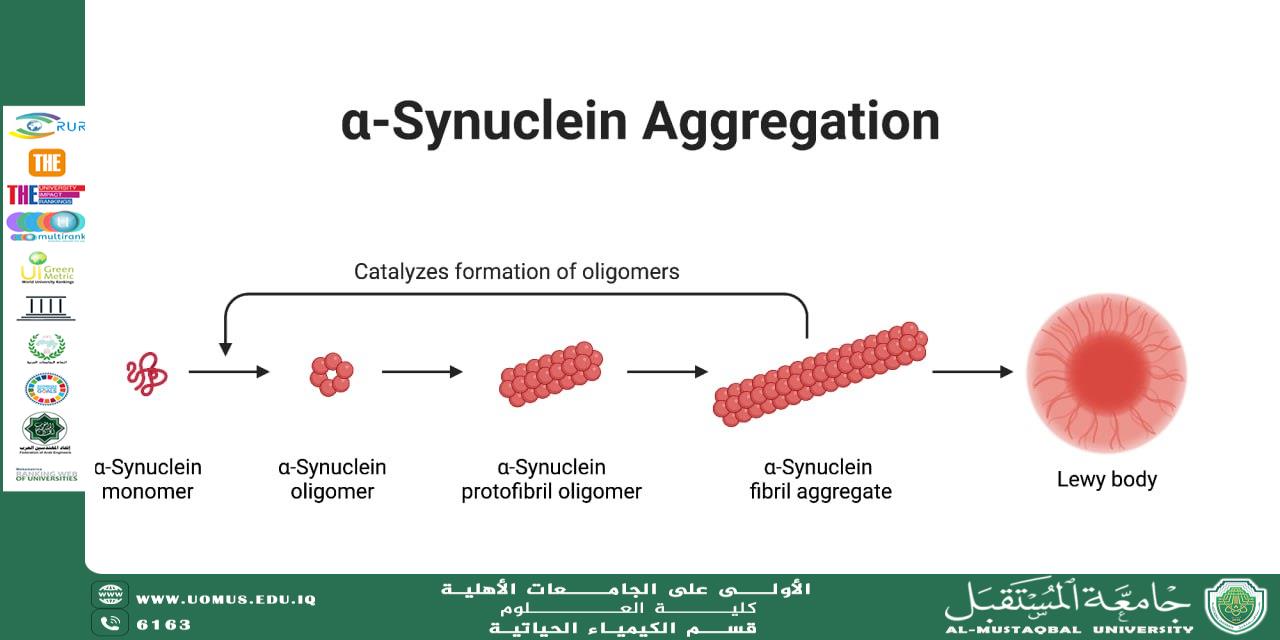
تمر عملية التجمع البروتيني بعدة مراحل:
التحول البنيوي من البنية الأصلية إلى شكل غير مستقر
تكوّن أوليغوميرات قابلة للذوبان
تشكّل ليفيات أميلويدية غير قابلة للذوبان
تراكم لويحات مرضية داخل النسيج العصبي
ويُعتقد أن المرحلة الأوليغوميرية هي الأكثر سمّية للخلايا العصبية، حيث تؤثر على:
نفاذية الأغشية الخلوية
وظيفة الميتوكوندريا
الإشارات العصبية المشبكية
وهنا يبرز دور الطرد المركزي التحليلي في الكشف الدقيق عن هذه المراحل المبكرة.
الدور التقني للطرد المركزي التحليلي (AUC)
يوفر الطرد المركزي التحليلي إمكانية دراسة البروتينات في حالتها الطبيعية داخل المحلول دون الحاجة إلى وسم فلوري أو تعديل كيميائي. ومن خلال قياس معامل الترسيب، يمكن:
التفريق بين المونوميرات والأوليغوميرات
تحديد الكتلة الجزيئية الفعلية للمجاميع
تحليل التوزيع الحجمي للجسيمات
دراسة الحركية الزمنية لعملية التجمع
كما يسمح نمط Sedimentation Velocity برصد التغيرات السريعة في تكوين المجاميع، بينما يوفر Sedimentation Equilibrium تقديرًا دقيقًا للكتلة الجزيئية وتوازن التجمع.
التكامل مع تقنيات تحليلية أخرى
تزداد قوة الطرد المركزي التحليلي عند دمجه مع تقنيات أخرى مثل:
المجهر الإلكتروني النافذ (TEM) لتصوير الليفيات
التحليل الطيفي للفلورية لرصد التغيرات البنيوية
Dynamic Light Scattering لتحديد الحجم الهيدروديناميكي
Mass Spectrometry لتحليل البنية الجزيئية
يسمح هذا التكامل بفهم شامل للآلية المرضية من المستوى البنيوي إلى المستوى الوظيفي.
البعد التشخيصي المبكر
تُظهر الأبحاث الحديثة أن التغيرات في نمط تجمع البروتينات قد تسبق الأعراض السريرية بسنوات طويلة. لذلك يمكن استخدام معاملات الترسيب كـ:
مؤشرات حيوية مبكرة
أدوات لمتابعة تطور المرض
معايير لتقييم فعالية الأدوية المضادة للتجمع
كما يجري العمل على تطوير اختبارات قائمة على تحليل تجمعات البروتينات في السائل الدماغي الشوكي أو البلازما، مما قد يُحدث نقلة نوعية في التشخيص غير الجراحي.
التحديات البحثية
رغم الدقة العالية للتقنية، إلا أن هناك تحديات تشمل:
صعوبة محاكاة البيئة الخلوية الحقيقية في المختبر
الحاجة إلى تراكيز بروتينية دقيقة
تعقيد تحليل البيانات الرياضية
التداخل المحتمل بين أنواع مختلفة من المجاميع
لكن التطور في البرمجيات التحليلية والنمذجة الحاسوبية ساهم في تقليل هذه القيود.
الاتجاهات المستقبلية
يتجه البحث العلمي نحو:
دراسة التفاعل بين البروتينات المتجمعة والعوامل الخلوية الأخرى
تطوير جزيئات علاجية تستهدف المرحلة الأوليغوميرية تحديدًا
تطبيق تقنيات الطرد المركزي التحليلي في الفحص السريري المبكر
استخدام الذكاء الاصطناعي لتحليل أنماط التجمع وتوقع مسار المرض
وقد يُسهم ذلك في الانتقال من مرحلة التشخيص المتأخر إلى مرحلة التدخل الوقائي المبكر.
يمثل الطرد المركزي التحليلي أداة أساسية في فهم الديناميكيات الجزيئية لتجمع البروتينات المرتبطة بأمراض التنكس العصبي. ومن خلال قدرته على تحليل المراحل المبكرة للتجمع بدقة عالية، يفتح المجال لتطوير مؤشرات حيوية جديدة واستراتيجيات علاجية مبتكرة.
إن تعزيز البحث في هذا المجال داخل أقسام الكيمياء الحياتية يرسّخ الدور الأكاديمي في دعم الطب الجزيئي والوقاية المبكرة من الاضطرابات العصبية التنكسية.
جامعة المستقبل الاولى على الجامعات العراقية الاهلية