مقالة علمية للتدريسية م.د داليا شاكر عبيدة بعنوان موت الخلايا المبرمج (Apoptosis): الآليات الحيوية والأهمية الفسيولوجية والمرضية
مقدمة
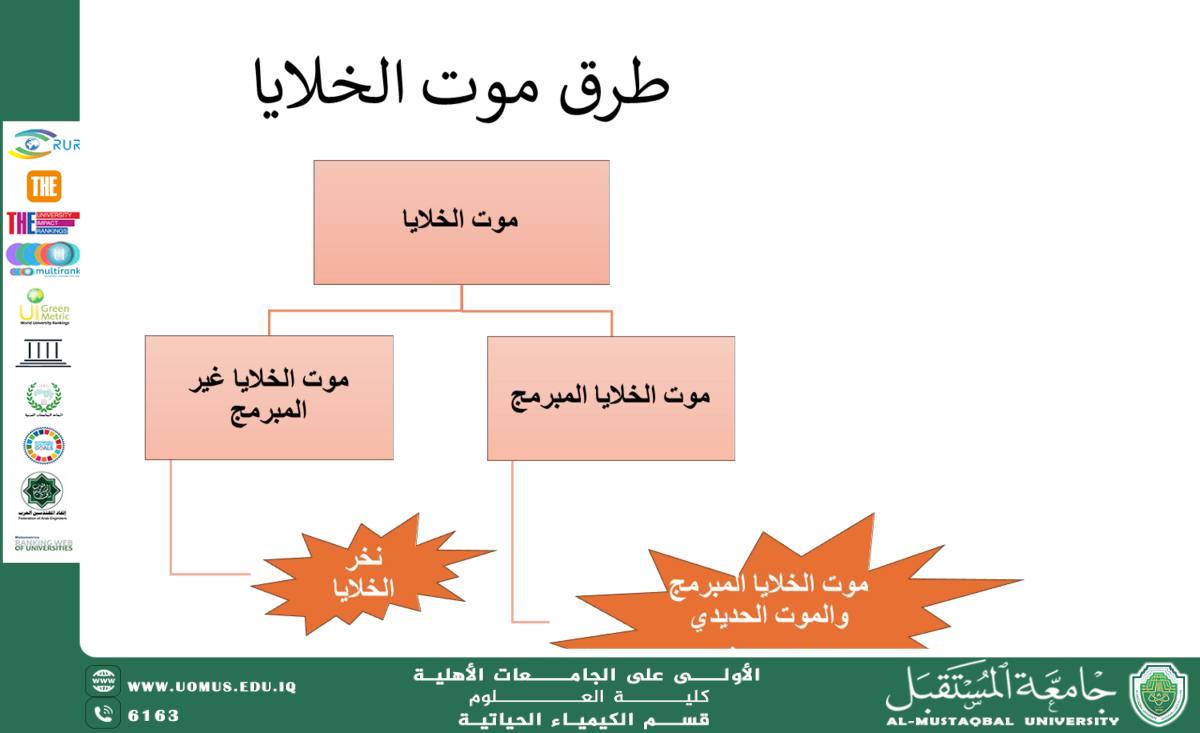
يُعدّ موت الخلايا المبرمج (Apoptosis) عملية حيوية منظمة تمكّن الكائنات متعددة الخلايا من الحفاظ على توازن الأنسجة وسلامة الكائن الحي. على عكس الموت الخلوي غير المنظم (Necrosis)، يتميز الاستماتة بكونها عملية دقيقة تُدار بواسطة مسارات جزيئية محددة، تؤدي إلى التخلص من الخلايا غير المرغوب فيها دون إحداث استجابة التهابية. وقد حظيت هذه الظاهرة باهتمام علمي واسع نظرًا لدورها الجوهري في النمو، والمناعة، والوقاية من السرطان.
تعريف موت الخلايا المبرمج
الاستماتة هي شكل من أشكال الموت الخلوي الفسيولوجي الذي يحدث نتيجة تنشيط داخلي أو خارجي لمسارات إشارات خلوية تؤدي إلى تدمير الخلية ذاتيًا بطريقة منظمة. تتميز هذه العملية بتكثف الكروماتين، وتجزؤ الحمض النووي (DNA)، وانكماش الخلية، وتكوين أجسام استماتية يتم ابتلاعها بواسطة الخلايا البلعمية دون إحداث ضرر للنسيج المحيط.
الخصائص المورفولوجية والكيميائية الحيوية
تشمل السمات المميزة لموت الخلايا المبرمج:
• انكماش الخلية وفقدان شكلها الطبيعي
• تكثف الكروماتين وتجزؤ النواة
• تكوّن حويصلات غشائية تُعرف بالأجسام الاستماتية
• تنشيط إنزيمات خاصة تُسمى الكاسبيزات (Caspases)
• غياب الاستجابة الالتهابية
1. المسار الداخلي (الميتوكوندري)
ينشأ هذا المسار نتيجة إشارات داخلية مثل تلف الـDNA، أو الإجهاد التأكسدي، أو نقص عوامل النمو. تلعب الميتوكوندريا دورًا محوريًا عبر تحرير السيتوكروم c إلى السيتوبلازم، مما يؤدي إلى تكوين معقّد يُفعّل الكاسبيز-9، ومن ثم الكاسبيزات التنفيذية مثل الكاسبيز-3.
2. المسار الخارجي (مستقبلات الموت)
يبدأ هذا المسار عندما ترتبط جزيئات خارجية (مثل Fas ligand أو TNF-α) بمستقبلات الموت على سطح الخلية. يؤدي ذلك إلى تنشيط الكاسبيز-8، الذي يُطلق سلسلة تفاعلات تنتهي بموت الخلية.
3. المسار المعتمد على الخلايا التائية
تستخدم الخلايا التائية السامة آليات خاصة (مثل الغرانزيمات) لتحفيز الاستماتة في الخلايا المصابة بالفيروسات أو الخلايا السرطانية.
الدور الفسيولوجي لموت الخلايا المبرمج
يؤدي موت الخلايا المبرمج وظائف أساسية، من أبرزها:
• تنظيم النمو الجنيني وتشكيل الأعضاء
• الحفاظ على توازن عدد الخلايا في الأنسجة
• إزالة الخلايا التالفة أو المصابة بالعدوى
• منع تكوّن الأورام عبر التخلص من الخلايا غير الطبيعية
العلاقة بين موت الخلايا المبرمج والأمراض
يؤدي الخلل في تنظيم الاستماتة إلى العديد من الأمراض:
• نقص الاستماتة: يساهم في تطور السرطان وأمراض المناعة الذاتية
• زيادة الاستماتة: ترتبط بأمراض التنكس العصبي مثل ألزهايمر وباركنسون
• أمراض القلب: تلعب الاستماتة دورًا في تلف عضلة القلب بعد نقص التروية
التطبيقات الطبية والعلاجية
أدى فهم آليات موت الخلايا المبرمج إلى تطوير استراتيجيات علاجية حديثة، خاصة في مجال السرطان، حيث تهدف بعض الأدوية إلى تحفيز الاستماتة في الخلايا السرطانية المقاومة للعلاج. كما يجري البحث في استهداف الكاسبيزات وبروتينات عائلة Bcl-2 كوسائل علاجية واعدة.
خاتمة
يمثل موت الخلايا المبرمج حجر الأساس في الحفاظ على الاتزان الحيوي للكائنات متعددة الخلايا. إن الفهم المتعمق لهذه العملية لا يساهم فقط في تفسير آليات النمو والتطور، بل يفتح آفاقًا واسعة لتطوير علاجات مبتكرة للأمراض المستعصية، مما يجعل الاستماتة محورًا أساسيًا في أبحاث الطب الحيوي الحديثة
جامعة المستقبل الأولى على الجامعات العراقية الأهلية