الهندسة الجزيئية للرقابة المناعية ضد السرطان
في المشهد المتطور لعلم الأورام الحديث، تحول التركيز من التدمير العشوائي للخلايا (العلاج الكيميائي) إلى التعديل الدقيق للجهاز المناعي البشري. إن ثورة "المناعة الورمية" (Immuno-Oncology) ليست مجرد علاج لمرض، بل هي استعادة لوظيفة بيولوجية فُقدت في التعرف على الخلايا الشاذة.
أولاً: دورة الرقابة المناعية: التعرف والتحفيز
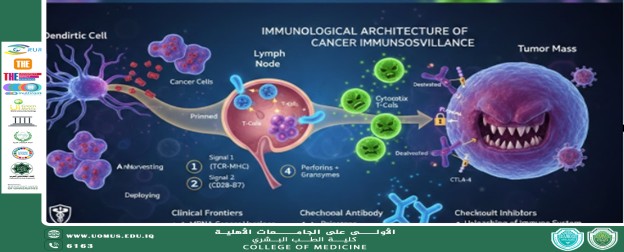
تبدأ المعركة ضد التنشؤ الأورامي بدورة مستمرة من المراقبة. وكما توضح النماذج الجزيئية الحالية، تبدأ العملية بـ حصاد المستضدات (Antigen Harvesting):
تكامل الخلايا الغصنية (Dendritic Cells): عندما تمر الخلايا السرطانية بحالة إجهاد أو استقلاب، تفرز مستضدات مرتبطة بالأورام (TAAs). تقوم الخلايا الغصنية—وهي الخلايا المحترفة في تقديم المستضد—بالتقاط هذه العلامات.
شرط "الإشارة المزدوجة": في العقد الليمفاوية الإقليمية، تقدم هذه الخلايا المستضدات للخلايا التائية (T-cells) عبر معقد التوافق النسيجي الكبير (MHC). ولتحويل الخلية التائية من حالة "خاملة" إلى "فعالة"، يجب توفر إشارتين:
الإشارة 1: ارتباط مستقبل الخلية التائية (TCR) بمعقد (MHC-Antigen).
الإشارة 2 (التحفيز المشترك): التفاعل بين بروتينات B7 على الخلية المقدمة للمستضد وبروتين CD28 على الخلية التائية. بدون هذه الإشارة الثانية، تدخل الخلية التائية في حالة وهن مناعي (Anergy).
ثانياً: الانتشار ومرونة الاستجابة
بمجرد تحفيزها، يتم إرسال أسطول متخصص إلى البيئة الدقيقة للورم (TME):
الخلايا التائية القاتلة (CD8+): هي المنفذ الرئيسي، حيث تستخدم البيرفورين (Perforins) لثقب غشاء الخلية السرطانية، والجرانزيمات (Granzymes) لبدء شلال "الكاسبيز" الذي يؤدي لموت الخلية المبرمج (Apoptosis).
دور السيتوكينات: تفرز الخلايا التائية المساعدة (CD4+) مواد مثل (Interferon-gamma) و(Interleukin-2)، والتي تعمل كمضخمات حيوية لاستدعاء الخلايا القاتلة الطبيعية (NK cells) والبالعات.
ثالثاً: آليات الهروب:
استغلال نقاط التفتيش التحدي الأكبر في علم الأورام السريري هو التمويه المناعي. الأورام ليست أهدافاً سلبية؛ بل تعمل بنشاط على "إسكات" الاستجابة المناعية عبر اختطاف مسارات تثبيط طبيعية مخصصة أصلاً لمنع أمراض المناعة الذاتية.
محور PD-1/PD-L1: تقوم الأورام غالباً بالتعبير المفرط عن بروتين PD-L1. عندما يرتبط هذا البروتين بمستقبل PD-1 الموجود على الخلية التائية النشطة، فإنه يرسل إشارة تثبيط—وهي بمثابة "صافرة توقف" جزيئية تجعل الخلية التائية غير فعالة.
مسار CTLA-4: تستغل بعض الأورام مسار CTLA-4 للتغلب على إشارة التحفيز المشترك، مما يمنع تنشيط الخلايا التائية في المراحل الأولى داخل العقد الليمفاوية.
رابعاً: الترجمة السريرية: عصر الأجسام المضادة أحادية النسيلة
لقد أدى الفهم العميق لهذه المسارات البيولوجية إلى تطوير ما يُعرف بـ مثبطات نقاط التفتيش المناعية (ICIs). ومن خلال استخدام أجسام مضادة أحادية النسيلة (Monoclonal Antibodies) مصممة هندسياً لغلق مستقبلات PD-1 أو CTLA-4، أصبح بإمكاننا "تحرير المكابح" عن الجهاز المناعي وإعادة إطلاقه لمهاجمة الخلايا السرطانية.
لفتة سريرية لطلاب الطب (Clinical Pearl)
على النقيض من العلاج الكيميائي التقليدي، الذي يستهدف الخلايا سريعة الانقسام (مما يؤدي إلى تسمم جهازي شامل)، يركز العلاج المناعي على "نقطة التماس" بين الجهاز المناعي والورم. بناءً على ذلك، يُعد ملف الآثار الجانبية لهذا العلاج فريداً من نوعه؛ حيث يتجلى غالباً في صورة أعراض جانبية مرتبطة بالمناعة (irAEs)، مثل التهاب القولون، أو التهاب الرئة، أو التهاب الغدة الدرقية. تعكس هذه الحالات فقداناً موضعياً لخاصية "التسامح الذاتي" (Self-tolerance)، مما يجعل الجسم يهاجم أنسجته السليمة.
الخاتمة: معيار جديد للرعاية الصحية
مع المضي قدماً في عام 2026، أصبح دمج العلاج المناعي الدقيق (Precision Immunotherapy) هو المعيار السائد؛ حيث يتم تحليل التسلسل الجيني لورم المريض للتنبؤ بنوع "مثبطات نقاط التفتيش" الأكثر فعالية لحالته. بالنسبة لطبيب المستقبل، أصبحت دراسة علم الأورام الآن مرتبطة ارتباطاً وثيقاً ولا ينفصم بدراسة علم المناعة,
بقلم أ.م.د. عبدالحسين مزهر المعموري
جامعة المستقبل الاولى على الجامعات الاهلية
.