مقالة علمية للست حوراء بعنوان المحفزات الحيوية في الأنظمة البيوكيميائية
الإنزيمات هي جزيئات حيوية ذات طبيعة بروتينية في أغلبها، تعمل كمحفزات بيولوجية تزيد من سرعة التفاعلات الكيميائية داخل الخلايا دون أن تُستهلك أثناء التفاعل. تُعد الإنزيمات عنصرًا أساسيًا في استمرارية الحياة، إذ تتحكم في مسارات الأيض المختلفة مثل عمليات البناء الحيوي والهدم وإنتاج الطاقة وتنظيم الإشارات الخلوية. إن غياب الإنزيمات أو انخفاض نشاطها يؤدي إلى بطء شديد في التفاعلات الحيوية، ما يجعل استمرار العمليات الخلوية بالكفاءة المطلوبة أمرًا غير ممكن.
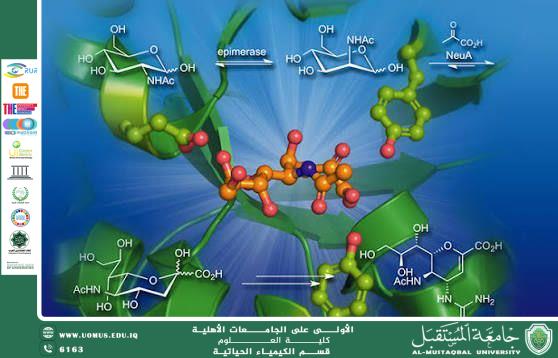
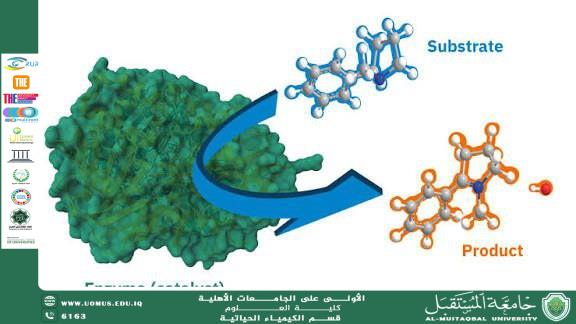
تعتمد آلية عمل الإنزيمات على وجود موقع نشط يُسمى (Active Site)، وهو جزء ثلاثي الأبعاد يتلاءم شكليًا وكيميائيًا مع المادة المتفاعلة المعروفة بالركيزة (Substrate). عند ارتباط الركيزة بالموقع النشط يتكون معقد إنزيم–ركيزة، مما يؤدي إلى خفض طاقة التنشيط اللازمة لحدوث التفاعل، وبالتالي تسريع معدل التفاعل. وقد فُسِّرت هذه العملية من خلال نموذجين رئيسيين هما نموذج القفل والمفتاح، ونموذج الملاءمة المستحثة، حيث يوضح الأخير أن الموقع النشط يتغير شكله قليلًا ليتلاءم مع الركيزة أثناء الارتباط.
تتميز الإنزيمات بدرجة عالية من التخصصية، إذ إن كل إنزيم غالبًا ما يعمل على ركيزة معينة أو مجموعة محددة من الركائز المتشابهة. ويرجع ذلك إلى البنية الفراغية الدقيقة للبروتين، والتي تحددها السلسلة الأمينية والترابطات الكيميائية الداخلية مثل الروابط الهيدروجينية وروابط ثنائي الكبريتيد. إن أي تغير في البنية الثلاثية قد يؤدي إلى فقدان النشاط الإنزيمي، وهي ظاهرة تُعرف بالتمسخ (Denaturation).
يتأثر نشاط الإنزيم بعدة عوامل فيزيائية وكيميائية، من أهمها درجة الحرارة، والرقم الهيدروجيني، وتركيز الركيزة، وتركيز الإنزيم. لكل إنزيم درجة حرارة مثلى يعمل عندها بأقصى كفاءة، وغالبًا ما تكون قريبة من درجة حرارة الجسم في الكائنات الحية العليا. كما أن لكل إنزيم رقمًا هيدروجينيًا أمثل، وأي انحراف كبير عنه قد يؤدي إلى تغير في شحنة الأحماض الأمينية بالموقع النشط وبالتالي انخفاض النشاط.
من الناحية الحركية، توصف العلاقة بين سرعة التفاعل وتركيز الركيزة بمعادلة ميكايليس–منتن، التي توضح مفهوم السرعة العظمى (Vmax) وثابت ميكايليس (Km)، وهو مؤشر على ألفة الإنزيم للركيزة. عندما يكون تركيز الركيزة عاليًا جدًا، تصل سرعة التفاعل إلى قيمة ثابتة نتيجة تشبع جميع المواقع النشطة.
تلعب المثبطات دورًا مهمًا في تنظيم النشاط الإنزيمي، وتنقسم إلى مثبطات تنافسية ترتبط بالموقع النشط وتنافس الركيزة، ومثبطات غير تنافسية ترتبط بموقع آخر في الإنزيم وتؤثر في بنيته الفراغية. وتُعد دراسة هذه المثبطات ذات أهمية كبيرة في تصميم الأدوية، إذ تعتمد العديد من العلاجات الدوائية على تثبيط إنزيمات محددة مرتبطة بالأمراض.
تصنف الإنزيمات دوليًا إلى ست فئات رئيسية وفق نوع التفاعل الذي تحفزه، وتشمل: إنزيمات الأكسدة والاختزال، وإنزيمات النقل، وإنزيمات التحلل المائي، وإنزيمات اللياز، وإنزيمات الإيزوميراز، وإنزيمات الربط. هذا التصنيف يُظهر التنوع الكبير في الوظائف البيوكيميائية التي تؤديها الإنزيمات داخل الكائن الحي.
لا تقتصر أهمية الإنزيمات على المجال الحيوي فحسب، بل تمتد إلى التطبيقات الصناعية والطبية، حيث تُستخدم في الصناعات الدوائية، وصناعة الأغذية، والتقنيات الحيوية، والتشخيص المختبري. كما تُعد المؤشرات الإنزيمية في الدم أدوات مهمة لتشخيص العديد من الأمراض، مثل إنزيمات الكبد وإنزيمات القلب.
في الختام، تمثل الإنزيمات حجر الأساس في الكيمياء الحيوية، إذ تُنظم وتسهل معظم التفاعلات داخل الخلية بكفاءة عالية ودقة تنظيمية معقدة. إن فهم طبيعة الإنزيمات وآليات عملها يسهم في تطوير مجالات الطب الحيوي والتكنولوجيا الحيوية، ويفتح آفاقًا واسعة للبحث العلمي والتطبيقات العلاجية المستقبلية.
جامعة المستقبل الاولى على الجامعات العراقية الاهلية