مقالة علمية لرئيس قسم الكيمياء الحياتية بعنوان الطرد المركزي بتدرج الكثافة في تحليل تحت أنواع البروتينات الدهنية وتقييم خطورة أمراض القلب
تُعد أمراض القلب والأوعية الدموية من الأسباب الرئيسية للوفاة عالميًا، ويُعتبر اضطراب استقلاب الدهون أحد أهم العوامل المساهمة في نشوء هذه الأمراض. وعلى الرغم من أن الفحوصات التقليدية لدهنيات الدم (الكوليسترول الكلي، LDL، HDL، والدهون الثلاثية) تُستخدم على نطاق واسع، إلا أنها لا تعكس دائمًا التعقيد الحقيقي لبنية البروتينات الدهنية وتحت أنواعها.
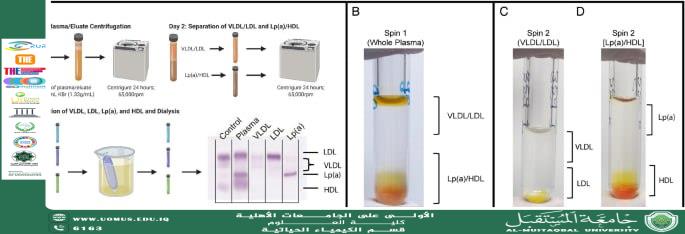
هنا تبرز أهمية تقنية الطرد المركزي بتدرج الكثافة (Density Gradient Ultracentrifugation) كأداة تحليلية دقيقة لفصل وتصنيف البروتينات الدهنية إلى تحت أنواع (Subfractions) ذات دلالة تشخيصية أعمق.
الأساس الفيزيائي والكيميائي للتقنية
تعتمد التقنية على مبدأ اختلاف الكثافة الطافية للجزيئات داخل وسط متدرج الكثافة (عادة السكروز أو أملاح البروميد). عند تطبيق قوة طرد مركزي عالية جدًا، تتحرك الجزيئات إلى الموضع الذي تتساوى فيه كثافتها مع كثافة الوسط المحيط، مكونة نطاقات منفصلة يمكن تحليلها بدقة.
تتحدد كثافة البروتينات الدهنية وفقًا لنسبة:
الدهون (كوليسترول، فوسفوليبيدات، ثلاثي الغليسريد)
البروتينات (Apolipoproteins)
ويؤدي اختلاف هذه النسب إلى تدرج كثافي يسمح بفصل:
الكيلوميكرونات
VLDL
LDL
HDL
تحليل تحت أنواع LDL وأهميتها السريرية
لم يعد LDL يُنظر إليه كوحدة متجانسة، بل يتكون من عدة تحت أنواع تختلف في:
الحجم
الكثافة
القابلية للأكسدة
القدرة على اختراق جدار الشرايين
وقد أظهرت الدراسات أن Small Dense LDL (sdLDL) يتميز بـ:
نفاذية أعلى للبطانة الوعائية
مقاومة أقل لمستقبلات LDL
قابلية أكبر للأكسدة
وهذا يجعله عاملًا رئيسيًا في تطور:
Atherosclerosis
Coronary artery disease
وبالتالي فإن قياس كمية sdLDL يوفر مؤشر خطورة أدق من قياس LDL الكلي.
دور HDL الوظيفي وليس الكمي فقط
رغم أن ارتفاع HDL يرتبط تقليديًا بانخفاض خطر أمراض القلب، إلا أن الدراسات الحديثة تشير إلى أن الوظيفة الحيوية لـ HDL (مثل قدرته على إزالة الكوليسترول من الخلايا – Reverse Cholesterol Transport) أكثر أهمية من تركيزه العددي.
يسمح الطرد المركزي بتدرج الكثافة بفصل HDL إلى تحت أنواع:
HDL2 (أكبر حجمًا)
HDL3 (أصغر وأكثر كثافة)
وقد تبين أن بعض التغيرات البنيوية في HDL قد تجعله “مختلاً وظيفيًا” في حالات الالتهاب المزمن والسكري.
الارتباط بالمتلازمة الأيضية والسكري
يرتبط ازدياد نسبة sdLDL وانخفاض HDL الفعال بوجود:
مقاومة الإنسولين
السمنة الحشوية
فرط ثلاثي الغليسريد
وتُعد هذه السمات مميزة لحالات مثل:
Type 2 diabetes
لذلك فإن التحليل المتقدم للبروتينات الدهنية يُعد أداة مهمة في تقييم المرضى ذوي الخطورة العالية حتى قبل ظهور مضاعفات قلبية واضحة.
التكامل مع تقنيات تحليلية أخرى
رغم أن الطرد المركزي بتدرج الكثافة يُعتبر المعيار الذهبي لفصل الليبوبروتينات، إلا أن دمجه مع تقنيات أخرى يعزز دقة التشخيص، مثل:
Nuclear Magnetic Resonance (NMR)
التحليل البروتيومي لأبوليبوبروتينات ApoB وApoA1
قياس المؤشرات الالتهابية مثل hs-CRP
هذا التكامل يسمح بفهم أعمق للآلية المرضية بدلاً من الاكتفاء بالمؤشرات التقليدية.
التحديات العملية
رغم دقتها العالية، تواجه التقنية بعض التحديات:
الحاجة إلى أجهزة طرد مركزي فائقة السرعة
طول زمن التحليل
التكلفة المرتفعة
صعوبة استخدامها في الفحوصات الروتينية واسعة النطاق
ولهذا فإن استخدامها يتركز غالبًا في المراكز البحثية أو الدراسات المتخصصة.
الآفاق المستقبلية
يتجه البحث العلمي حاليًا نحو:
تطوير طرق طرد مركزي مصغرة وسريعة
أتمتة عمليات الفصل والتحليل
استخدام الذكاء الاصطناعي لتحليل أنماط تحت الأنواع
اعتماد المؤشرات الجزيئية الدقيقة في الإرشادات السريرية المستقبلية
وقد يؤدي ذلك إلى انتقال تقييم خطورة أمراض القلب من نموذج تقليدي يعتمد على الكوليسترول الكلي إلى نموذج جزيئي متكامل قائم على البنية الوظيفية للبروتينات الدهنية.
يمثل الطرد المركزي بتدرج الكثافة أداة تحليلية متقدمة تمكّن من الكشف الدقيق عن التغيرات البنيوية والوظيفية في البروتينات الدهنية. ويساهم هذا النهج في تحسين تقييم خطورة أمراض القلب والشرايين من خلال تحليل تحت الأنواع ذات التأثير المرضي الأكبر.
جامعة المستقبل الاولى على الجامعات العراقية الاهلية